发布时间:2024-01-11 14:39:25
前 言
本标准代替GB/T 4789.10-2008《食品卫生微生物学检验 金黄色葡萄球菌检验》和
GB/T 4789.37-2008《食品卫生微生物学检验 金黄色葡萄球菌计数》。
本标准与GB/T 4789.10-2008 和GB/T4789.37-2008 相比,主要修改如下:
——修改了标准的中英文名称;
——修改了范围;
——规范了样品制备过程;
——增加了计算公式中系数1.1 的解释;
——修改了附录A 中胰酪胨大豆肉汤的名称,规范为10%氯化钠胰酪胨大豆肉汤;
——增加了第二法金黄色葡萄球菌 Baird-Parker 平板计数和第三法金黄色葡萄球菌MPN 计数。
本标准的附录A、附录B、附录C 是规范性附录。
本标准所代替标准的历次版本发布情况为:
——GB 4789.10-84、GB 4789.10-1994、GB/T 4789.10-2003、GB/T 4789.10-2008。
——GB/T 4789.37-2008。
食品安全国家标准
食品微生物学检验 金黄色葡萄球菌检验
1 范围
本标准规定了食品中金黄色葡萄球菌(Staphylococcus aureus)的检验方法。
本标准第一法适用于食品中金黄色葡萄球菌的定性检验;第二法适用于金黄色葡萄球菌含量较高的食品中金黄色葡萄球菌的计数;第三法适用于金黄色葡萄球菌含量较低而杂菌含量较高的食品中金黄色葡萄球菌的计数。
2 设备和材料
除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:
2.1 恒温培养箱:36 ℃±1 ℃。
2.2 冰箱:2 ℃~5 ℃。
2.3 恒温水浴箱:37 ℃~65 ℃。
2.4 天平:感量0.1 g。
2.5 均质器。
2.6 振荡器。
2.7 无菌吸管:1 mL(具0.01 mL 刻度)、10 mL(具0.1 mL 刻度)或微量移液器及吸头。
2.8 无菌锥形瓶:容量100 mL、500 mL。
2.9 无菌培养皿:直径90 mm。
2.10 注射器:0.5 mL。
2.11 pH 计或pH 比色管或精密pH 试纸。
3 培养基和试剂
3.1 10 %氯化钠胰酪胨大豆肉汤:见附录A 中A.1。
3.2 7.5 %氯化钠肉汤:见附录A 中A.2。
3.3 血琼脂平板:见附录A 中A.3。
3.4 Baird-Parker 琼脂平板:见附录A 中A.4。
3.5 脑心浸出液肉汤(BHI) :见附录A 中A.5。
3.6 兔血浆:见附录A 中A.6。
3.7 稀释液:磷酸盐缓冲液:见附录A 中A.7。
3.8 营养琼脂小斜面:见附录A 中A.8。
3.9 革兰氏染色液:见附录A 中A.9。
3.10 无菌生理盐水:见附录A 中A.10。
第一法 金黄色葡萄球菌定性检验
4 检验程序
金黄色葡萄球菌定性检验程序见图1。
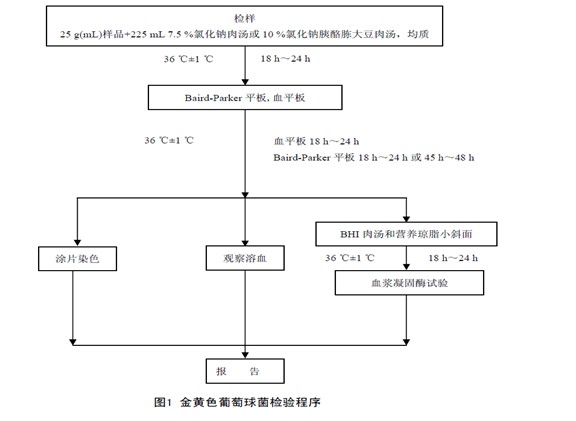
5 操作步骤
5.1 样品的处理
称取25 g样品至盛有225 mL 7.5 %氯化钠肉汤或10 %氯化钠胰酪胨大豆肉汤的无菌均质杯内,8000 r/min~10000 r/min 均质1 min~2min,或放入盛有225 mL 7.5 %氯化钠肉汤或10 %氯化钠胰酪胨大豆肉汤的无菌均质袋中,用拍击式均质器拍打1 min~2 min。若样品为液态,吸取25 mL 样品至盛有225 mL 7.5 %氯化钠肉汤或10 %氯化钠胰酪胨大豆肉汤的无菌锥形瓶(瓶内可预置适当数量的无菌玻璃珠)中,振荡混匀。
5.2 增菌和分离培养
5.2.1将上述样品匀液于36 ℃±1 ℃培养18 h~24 h。金黄色葡萄球菌在7.5%氯化钠肉汤中呈混浊生长,污染严重时在10%氯化钠胰酪胨大豆肉汤内呈混浊生长。
5.2.2将上述培养物,分别划线接种到Baird-Parker 平板和血平板,血平板36 ℃±1 ℃培养18 h~24 h。Baird-Parker平板36 ℃±1 ℃培养18 h~24 h 或45 h~48 h。
5.2.3金黄色葡萄球菌在Baird-Parker 平板上,菌落直径为2 mm~3 mm,颜色呈灰色到黑色,边缘为淡色,周围为一混浊带,在其外层有一透明圈。用接种针接触菌落有似奶油至树胶样的硬度,偶然会遇到非脂肪溶解的类似菌落;但无混浊带及透明圈。长期保存的冷冻或干燥食品中所分离的菌落比典型菌落所产生的黑色较淡些,外观可能粗糙并干燥。在血平板上,形成菌落较大,圆形、光滑凸起、湿润、金黄色(有时为白色),菌落周围可见完全透明溶血圈。挑取上述菌落进行革兰氏染色镜检及血浆凝固酶试验。
5.3 鉴定
5.3.1染色镜检:金黄色葡萄球菌为革兰氏阳性球菌,排列呈葡萄球状,无芽胞,无荚膜,直径约为0.5 μm~1 μm。
5.3.2血浆凝固酶试验:挑取、Baird-Parker 平板或血平板上可疑菌落1 个或以上,分别接种到5 mL BHI和营养琼脂小斜面,36 ℃±1 ℃培养18 h~24 h。
取新鲜配置兔血浆0.5 mL,放入小试管中,再加入BHI 培养物0.2 mL~0.3 mL,振荡摇匀,置36℃±1 ℃温箱或水浴箱内,每半小时观察一次,观察6 h,如呈现凝固(即将试管倾斜或倒置时,呈现凝块)或凝固体积大于原体积的一半,被判定为阳性结果。同时以血浆凝固酶试验阳性和阴性葡萄球菌菌株的肉汤培养物作为对照。也可用商品化的试剂,按说明书操作,进行血浆凝固酶试验。结果如可疑,挑取营养琼脂小斜面的菌落到5 mL BHI,36 ℃±1 ℃培养18 h~48 h,重复试验。
5.4 葡萄球菌肠毒素的检验
可疑食物中毒样品或产生葡萄球菌肠毒素的金黄色葡萄球菌菌株的鉴定,应按附录B检测葡萄球菌肠毒素。
6 结果与报告
6.1 结果判定:符合5.2.3、5.3,可判定为金黄色葡萄球菌。
6.2 结果报告:在25 g(mL)样品中检出或未检出金黄色葡萄球菌。
第二法 金黄色葡萄球菌 Baird-Parker平板计数
7 检验程序
金黄色葡萄球菌平板计数程序见图2。
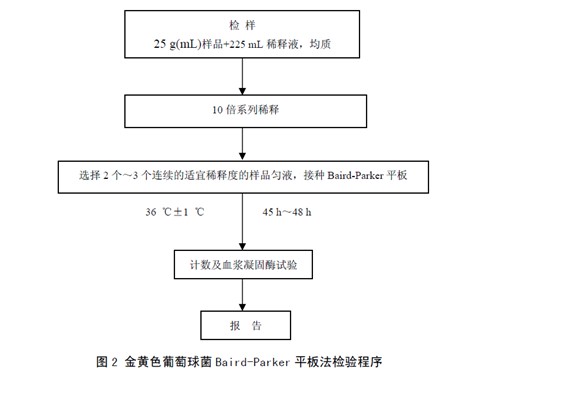
8 操作步骤
8.1 样品的稀释
8.1.1固体和半固体样品:称取25 g样品置盛有225 mL磷酸盐缓冲液或生理盐水的无菌均质杯内,8000r/min~10000 r/min均质1 min~2min,或置盛有225 mL稀释液的无菌均质袋中,用拍击式均质器拍打1min~2 min,制成1:10的样品匀液。
8.1.2液体样品:以无菌吸管吸取25 mL样品置盛有225 mL磷酸盐缓冲液或生理盐水的无菌锥形瓶(瓶内预置适当数量的无菌玻璃珠)中,充分混匀,制成1:10的样品匀液。
8.1.3用1 mL 无菌吸管或微量移液器吸取1:10 样品匀液1 mL,沿管壁缓慢注于盛有9 mL 稀释液的无菌试管中(注意吸管或吸头尖端不要触及稀释液面),振摇试管或换用1 支1 mL 无菌吸管反复吹打使其混合均匀,制成1:100 的样品匀液。
8.1.4按8.1.3 操作程序,制备10 倍系列稀释样品匀液。每递增稀释一次,换用1 次1 mL 无菌吸管或吸头。
8.2 样品的接种
根据对样品污染状况的估计,选择2 个~3 个适宜稀释度的样品匀液(液体样品可包括原液),在进行10 倍递增稀释时,每个稀释度分别吸取1 mL 样品匀液以0.3 mL、0.3 mL、0.4 mL接种量分别加入三块Baird-Parker 平板,然后用无菌L棒涂布整个平板,注意不要触及平板边缘。使用前,如Baird-Parker平板表面有水珠,可放在25 ℃~50 ℃的培养箱里干燥,直到平板表面的水珠消失。
8.3 培养
8.3.1.1 在通常情况下,涂布后,将平板静置10 min,如样液不易吸收,可将平板放在培养箱36 ℃±1℃培养1h;等样品匀液吸收后翻转平皿,倒置于培养箱,36 ℃±1 ℃培养,45 h~48 h。
8.4 典型菌落计数和确认
8.4.1金黄色葡萄球菌在Baird-Parker 平板上,菌落直径为2 mm~3 mm,颜色呈灰色到黑色,边缘为淡色,周围为一混浊带,在其外层有一透明圈。用接种针接触菌落有似奶油至树胶样的硬度,偶然会遇到非脂肪溶解的类似菌落;但无混浊带及透明圈。长期保存的冷冻或干燥食品中所分离的菌落比典型菌落所产生的黑色较淡些,外观可能粗糙并干燥。
8.4.2选择有典型的金黄色葡萄球菌菌落的平板,且同一稀释度3 个平板所有菌落数合计在20 CFU~200 CFU 之间的平板,计数典型菌落数。如果:
a)只有一个稀释度平板的菌落数在20 CFU~200 CFU之间且有典型菌落,计数该稀释度平板上的典型菌落;
b) 最低稀释度平板的菌落数小于20 CFU 且有典型菌落,计数该稀释度平板上的典型菌落;
c)某一稀释度平板的菌落数大于200 CFU 且有典型菌落,但下一稀释度平板上没有典型菌落,应计数该稀释度平板上的典型菌落;
d) 某一稀释度平板的菌落数大于200 CFU 且有典型菌落,且下一稀释度平板上有典型菌落,但其平板上的菌落数不在20 CFU~200 CFU 之间,应计数该稀释度平板上的典型菌落;
以上按公式(1)计算。
e) 2 个连续稀释度的平板菌落数均在20 CFU~200 CFU 之间,按公式(2)计算。
8.4.3从典型菌落中任选5 个菌落(小于5 个全选),分别按5.3.2 做血浆凝固酶试验。
9 结果计算:
公式(1):
T = AB/CD ………………………………………………………………… (1)
式中:
T——样品中金黄色葡萄球菌菌落数;
A——某一稀释度典型菌落的总数;
B——某一稀释度血浆凝固酶阳性的菌落数;
C——某一稀释度用于血浆凝固酶试验的菌落数;
d——稀释因子。
公式(2):
T=(A1B1/C1+A2B2/C2)/1.1d………………………(2)
式中:
T ——样品中金黄色葡萄球菌菌落数;
A1——第一稀释度(低稀释倍数)典型菌落的总数;
A2——第二稀释度(高稀释倍数)典型菌落的总数;
B1——第一稀释度(低稀释倍数)血浆凝固酶阳性的菌落数;
B2——第二稀释度(高稀释倍数)血浆凝固酶阳性的菌落数;
C1——第一稀释度(低稀释倍数)用于血浆凝固酶试验的菌落数;
C2——第二稀释度(高稀释倍数)用于血浆凝固酶试验的菌落数;
1.1——计算系数;
d ——稀释因子(第一稀释度)。
10 结果与报告
根据Baird-Parker平板上金黄色葡萄球菌的典型菌落数,按9中公式计算,报告每g(mL)样品中金黄色葡萄球菌数,以CFU/g(mL)表示;如T值为0,则以小于1乘以最低稀释倍数报告。
第三法 金黄色葡萄球菌MPN计数
11 检验程序
金黄色葡萄球菌MPN计数程序见图3。
12 操作步骤
12.1 样品的稀释
按8.1进行。
12.2 接种和培养
12.2.1根据对样品污染状况的估计,选择3 个适宜稀释度的样品匀液(液体样品可包括原液),在进行10 倍递增稀释时,每个稀释度分别吸取1 mL 样品匀液接种到10%氯化钠胰酪胨大豆肉汤管,每个稀释度接种3管,将上述接种物于36 ℃±1 ℃培养45 h~48 h。
12.2.2用接种环从有细菌生长的各管中,移取1环,分别接种Baird-Parker平板,36 ℃±1 ℃培养45 h~48 h。
12.3 典型菌落确认
12.3.1见8.4.1。
12.3.2从典型菌落中至少挑取1 个菌落接种到BHI肉汤和营养琼脂斜面,36 ℃±1 ℃培养18 h~24 h。进行血浆凝固酶试验,见5.3.2。
13 结果与报告
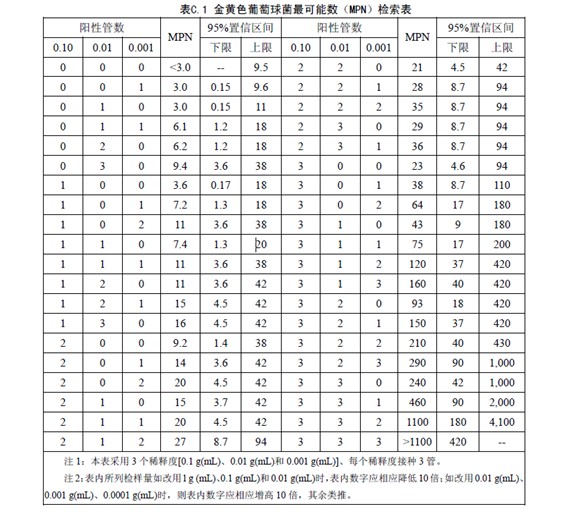
计算血浆凝固酶试验阳性菌落对应的管数,查MPN 检索表(见附录C),报告每g(mL)样品中金黄色葡萄球菌的最可能数,以MPN/g(mL)表示。
附录A (规范性附录)
培养基和试剂
A.1 10%氯化钠胰酪胨大豆肉汤
A.1.1成分
胰酪胨(或胰蛋白胨)17.0 g
植物蛋白胨(或大豆蛋白胨)3.0 g
氯化钠100.0 g
磷酸氢二钾2.5 g
丙酮酸钠10.0 g
葡萄糖2.5 g